Универсальные поурочные разработки по Физике 8 класс к учебнику А. В. Перышкина
Агрегатные состояния вещества - Изменение агрегатных состояний вещества
Цель: изучить физические особенности в строении и свойствах различных веществ.
Демонстрации: модели кристаллических решеток; наблюдение за процессами испарения, плавления и кристаллизации; набор кристаллических и аморфных тел.
Ход урока
I. Анализ результатов контрольной работы
Перед началом изучения новой темы необходимо провести краткий анализ результатов контрольной работы, обсудить наиболее типичные ошибки, рассмотреть решения некоторых задач у доски.
II. Изучение нового материала
План изложения нового материала:
1. Три агрегатных состояния вещества.
2. Виды перехода из одного агрегатного состояния в другое.
1. Изложение нового материала следует начать с демонстрации простейшего опыта. В прозрачном сосуде с водой плавают кусочки льда, и сосуд плотно закрыт крышкой.
Очевидно, что температура смеси примерно равна 0 °С. То есть возможна такая ситуация, когда вещество одновременно находится в твердом, жидком и газообразном состоянии.
Любое вещество, состоящее из атомов или молекул, может находиться в одном из трех агрегатных состояний: а) твердом; б) жидком или в) газообразном.
- Что же отличает одно агрегатное состояние вещества от другого?
- Каковы особенности молекулярного строения газов, жидкостей и твердых тел? (Прежде чем продолжить объяснение, желательно выслушать мнения учащихся.)
На примере моделей кристаллических решеток видно, что в твердом состоянии положение молекул упорядочено. Они не могут свободно перемещаться по телу.
Молекулы жидкости не имеют такой структуры в расположении, силы взаимодействия у них меньше, чем у молекул твердых тел, и поэтому даже под действием небольших внешних сил они легко перемещаются. Жидкости обладают текучестью.
Молекулы газа еще слабее связаны друг с другом, и поэтому перемещаются по всему объему с большими скоростями. При этом они часто сталкиваются друг с другом. Это можно наблюдать на примере распространения запаха духов по комнате.
Делается вывод: во-первых, в разных агрегатных состояниях расположение атомов и молекул различно; во-вторых, внутренняя энергия одинаковых масс твердого тела, жидкости и газа при одинаковых температурах различна.
В ознакомительном плане можно рассказать учащимся об аморфных телах, которые обладают свойствами твердых тел (прочность, хрупкость, твердость) и свойствами жидкостей (текучесть, не сохраняют формы с течением времени).
2. Процесс перехода вида «твердое вещество → жидкость → газ» связан с увеличением внутренней энергии. Значит, в таких превращениях вещество поглощает тепло, и кинетическая энергия движения молекул возрастает, то есть: v↑, ΔU > 0.
А в переходе вида «газ → жидкость → твердое вещество» процесс перехода идет с выделением тепла. При этом скорость молекул и внутренняя энергия уменьшаются, то есть: v↓, ΔU < 0.
Иногда бывает так, что вещество из данного агрегатного состояния сразу переходит в иное, минуя жидкую фазу. Процесс перехода из твердого состояния в газообразное называется сублимацией или возгонкой. Сублимирует кусочек льда в морозный день. Сырое белье замерзает на ветру в мороз, а через сутки становится сухим - ледяная корка исчезает. Также сублимирует угольная кислота в брикетах. Вообще любое тело в твердом состоянии, если оно имеет запах, сублимирует.
Процесс перехода вещества из твердого состояния в жидкое называется плавлением. Оно идет с поглощением тепла.
Процесс превращения жидкости в пар называется парообразованием. Это тоже требует количества теплоты извне.
Процесс превращения жидкости в твердое тело называется кристаллизацией. При этом вещество часть тепла отдает в окружающую среду.
Процесс превращения пара в жидкость называется конденсацией.
Очень интересным процессом является процесс, обратный сублимации, - десублимация. При этом вещество из газообразного состояния сразу переходит в жидкую фазу.
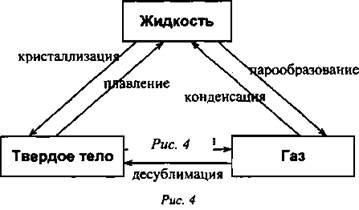
Таким образом, есть шесть процессов, которые определяют варианты перехода вещества из одного агрегатного состояния в другое (рис. 4): плавление, кристаллизация, парообразование, конденсация, сублимация, десублимация.
Домашнее задание
1. § 12 учебника; вопросы и задания к параграфу.
2. Сборник задач В. И. Лукашика, Е. В. Ивановой, № 1012, 1013.