Настольная книга учителя по химии 9 класс - поурочные разработки
Магний и щелочноземельные металлы - Урок 2 - Ответы - Формирование приемов умственной деятельности у учащихся в курсе химии 9 класса - Приложения
1. а) Названия элементов главной подгруппы II группы: магний, кальций, барий;
б) состав атомных частиц, соответствующих элементам главной подгруппы II группы: 4р, 5n, 4ē; 20р, 20n, 20ē;
в) электронные схемы, соответствующие атомам химических элементов главной подгруппы II группы:
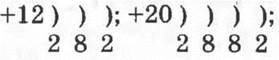
г) ![]() — изотопы химических элементов главной подгруппы II группы;
— изотопы химических элементов главной подгруппы II группы;
д) высшие оксиды элементов главной подгруппы II группы: CaO, MgO;
е) гидроксиды элементов главной подгруппы II группы: Са(ОН)2, Mg(OH)2.
2. Ва, Sr, Са, Mg, Be.
В указанной последовательности электроотрицательность увеличивается, восстановительные свойства уменьшаются, металлические свойства уменьшаются.
3*. Признаки, по которым можно объединять записанные вещества в группы: агрегатное состояние, цвет, запах, растворимость в воде, принадлежность к классам веществ, токсичность, определенные химические свойства, нахождение в природе. Например, для кальция:
• металлы: Na, Ва, Сu, Ag;
• простые вещества, образованные химическими элементами II группы главной подгруппы ПСХЭ: Mg, Be, Sr, Ва;
• простые вещества, образованные химическими элементами четвертого периода: К, Mn, Fe, Вr2;
• вещества, взаимодействующие с водой: Na, Na2O, СO2, Р2O5 и т. д.
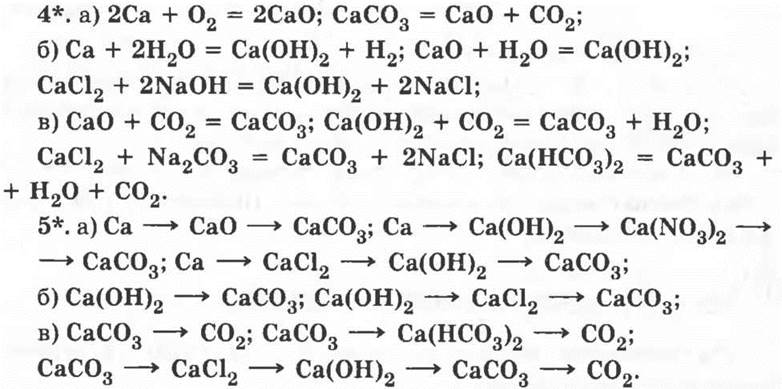
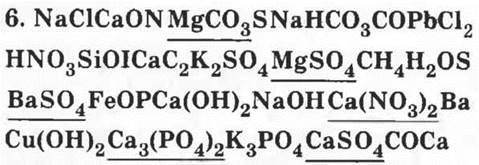
MgCO3 — карбонат магния (производство стекла, цемента, кирпича, в металлургии); MgSO4 — сульфат магния (в медицине — слабительное); BaSO4 — сульфат бария (в медицине — в рентгенодиагностике); Ca(NO3)2 — нитрат кальция (азотное удобрение); Са3(РO4)2 — фосфат кальция; CaSO4 — сульфат кальция (применяют в виде алебастра 2CaSO4 · Н2O в строительстве, в медицине — для наложения гипсовых повязок, получения слепков полости рта).
7*. Круг 1 — реакции 2, 4. Круг 2 — реакции 1, 3.
Область пересечения — реакция 5.
Уравнение реакции: ![]()
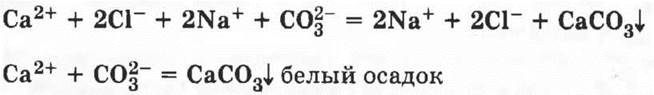
8. Ar(Mg) = 24 (таблица 19).
Таблица 19
|
Вещество |
Область применения |
||
|
В строительстве |
Реактив на оксид углерода (IV) |
Очистка свекловичного сока |
|
|
Гашеная известь |
|
7 |
3 |
|
Известковая вода |
6 |
|
1 |
|
Негашеная известь |
|
9 |
12 |
|
Известковое молоко |
11 |
5 |
|
2*.
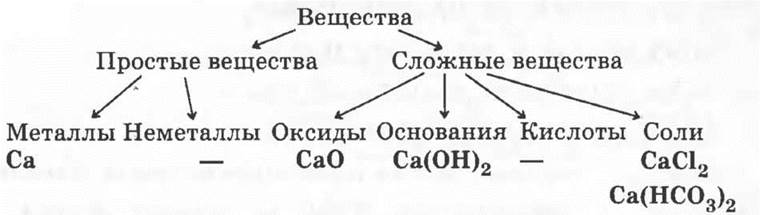
Основание классификации — состав веществ.
10. Для обозначения: а) химического элемента — 5 раз;
б) простого вещества — 2 раза.
11. O химических явлениях — 3 раза; о физических явлениях не упоминалось.



